蝙蝠是多种烈性病毒的天然宿主,能够无症状地携带多种哺乳动物烈性病毒,包括多次引起全球大流行的冠状病毒。在所有蝙蝠的科级分类群中,菊头蝠科蝙蝠的冠状病毒检出率最高。然而,关于菊头蝠染色体演化和免疫适应的分子机制,此前一直缺乏深入的系统性研究。
近日,广东省科学院动物研究所动物生态与进化研究中心联合武汉大学、英国伦敦玛丽女王大学合作,结合比较基因组学、群体基因组学、比较转录组学及细胞功能实验,揭示了菊头蝠染色体演化及其独特的免疫适应机制。
研究团队对包括皮氏菊头蝠和中华菊头蝠在内的5种蝙蝠进行了基因组测序和组装,并与已发表的其他哺乳动物基因组进行比较。研究发现,菊头蝠祖先可能有30对染色体,其染色体重排由基因组大片段重复事件驱动,促进了物种多样性分化。研究还发现,菊头蝠干扰素刺激基因ANXA2R和I型干扰素亚家族(IFN-δ和IFN-ω)发生适应性扩张,这些基因的扩张增强了蝙蝠的抗病毒能力。此外,研究揭示了菊头蝠与蝙蝠人畜共患病相关病毒的基因演化关系,发现多个与病毒受体相关的基因存在正选择或加速演化信号,包括SARS-CoV和SARS-CoV-2的受体基因ACE2,表明菊头蝠对病毒的易感性存在显著差异。
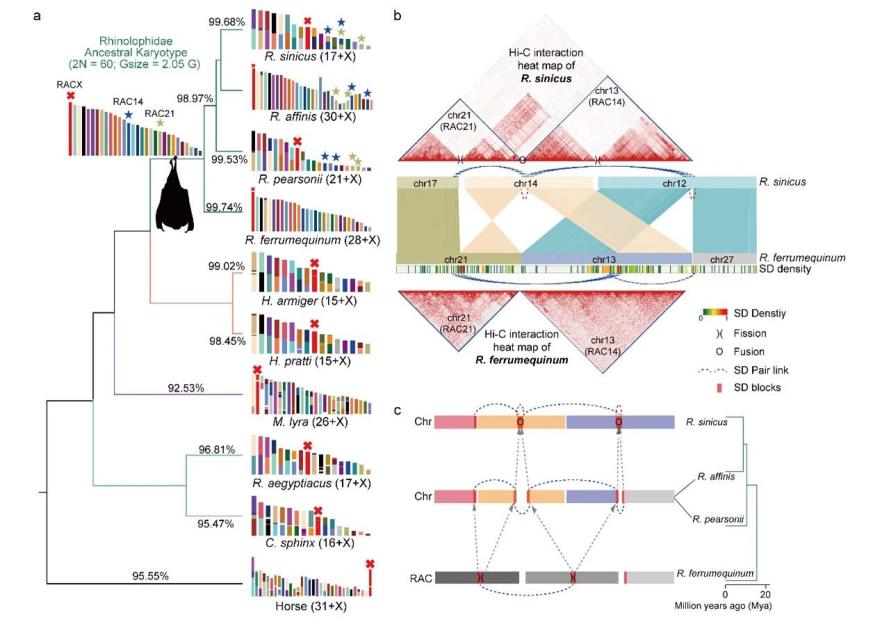
图1. 菊头蝠科蝙蝠染色体的演化
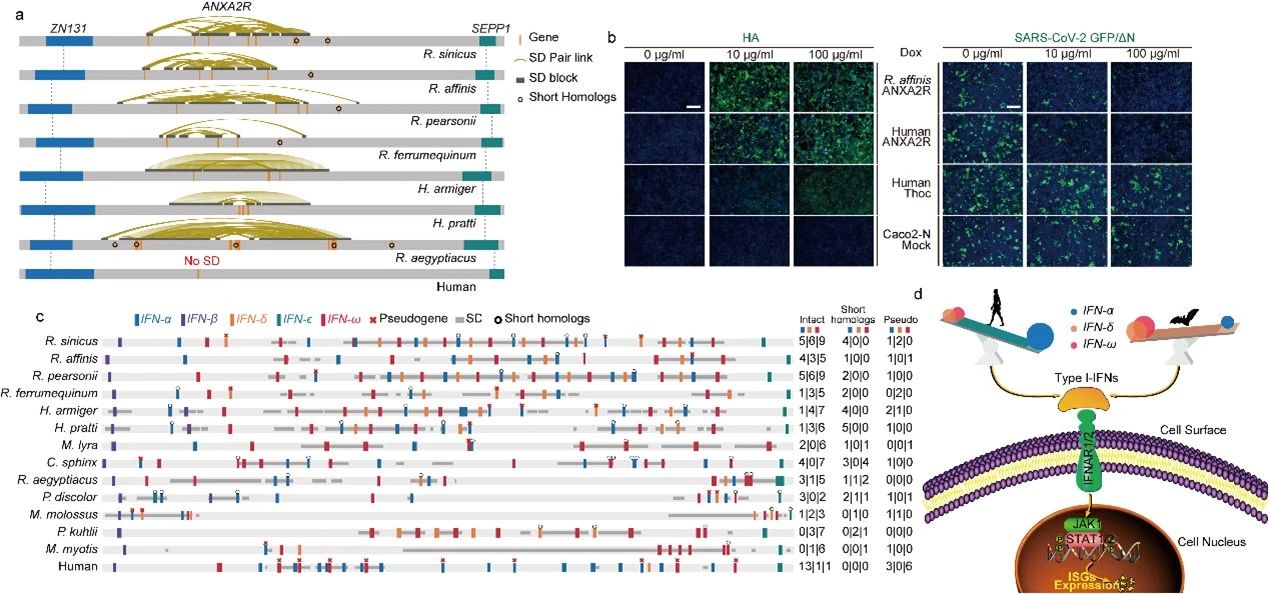
图2. 菊头蝠ANXA2R基因扩增和I型干扰素基因的多样性
该研究为菊头蝠的演化和免疫机制研究提供了新见解,也为人类抗病毒治疗策略的制定提供了理论依据,相关成果发表于Nature子刊Nature Ecology & Evolution(IF = 14.1),武汉大学博士毕业生田仕林和司竣宇以及广东省科学院动物研究所张礼标研究员为共同第一作者,武汉大学赵华斌教授和英国伦敦玛丽女王大学Stephen Rossiter教授为共同通讯作者。该研究得到广东省科技计划项目、国家自然科学基金、国家重点研发计划、广州国家实验室研发计划等项目的资助。
论文信息:Tian, S., Si, J., Zhang, L.et al.Comparative genomics provides insights into chromosomal evolution and immunological adaptation in horseshoe bats.Nat Ecol Evol(2025). https://doi.org/10.1038/s41559-025-02638-2
供稿:省科学院动物所
撰稿:张礼标
审稿:黄丹 陈金平 吴玉春
校稿:徐超 肖捷 章震
 附件下载:
附件下载: